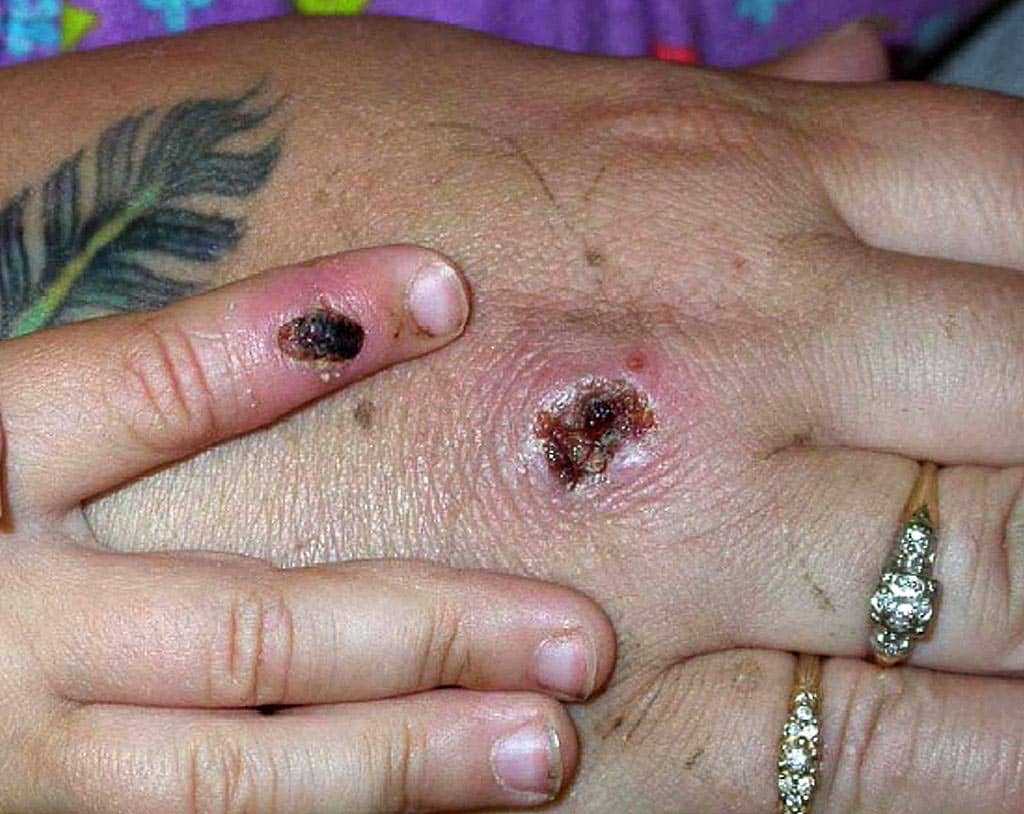
Date de rédaction de cet article: 21 mai 2022. Photo d’illustration: CDC
Suite à la détection du premier cas confirmé en Suisse, et face à la récente flambée médiatique concernant la variole de singe se tramant dans les médias, en réponse à la détection de cas en Europe, mais également en Amérique du Nord et en Australie, l’OMS ainsi que l’ECDC (European Center for Disease Control) et du US CDC se sont réuni afin de préparer une potentielle montée en puissance. En effet, cette soudaine détection de cas dans des zones non endémique (Afrique centrale et occidentale), dans une population masculine homosexuelle (en date de rédaction, l’ensemble des cas détectés était chez des patients HSH) n’ayant pas eu de voyage en zone endémique, est atypique. Occasionnellement détecté chez des patients ayant précédemment voyagé en Afrique centrale ou occidentale, cette atypicité, affectant une population en particulier, sans lien épidémiologique connu avec l’Afrique occidentale et centrale évoquent aux yeux des autorités internationales une transmission communautaire a large échelle.
Ce post a pour but de faire un bref rappel des caractéristiques de la variole de singe (Monkeypox), à but informatif.
Pour de plus amples lectures à son sujet, je vous invite à consulter le site de l’OMS, de l’ECDC.
Introduction
Résultat d’une infection par le virus zoonotique Monkeypox (famille des Orthopoxvirus), la variole du singe a été pour la première fois observé dans une colonie de singe en 1958 (d’où le nom Monkeypox). Détecté par la suite dans d’autres animaux (écureuils, rats, souris), ce n’est qu’en 1970 que le premier cas est détecté chez un jeune garçon de 9 ans vivant en République Démocratique du Congo. Depuis, d’occasionnels cas isolés et même quelques pandémies locales ont été rapportés par 11 pays d’Afrique (avec des donnes épidémiologiques occasionnellement peu fiables), principalement dans le basin du Congo et les forêts tropicales environnantes. Depuis 2017, 500 cas suspects et 200 cas confirmés (avec un taux de mortalité avoisinant les 3%) ont été enregistrés au Nigeria. Mais cette maladie n’affecte pas que les pays africains, et en 2003, les premiers cas hors Afrique sont enregistrés aux USA (70 patients), avec un mode de transmission lié aux chiens de prairie (genre de rongeur), eux-mêmes infectés par des rats venant du Gabon.
La transmission zoonotique est généralement le fruit d’un repas de viande d’animaux réservoirs pas assez cuits. D’humain en humain, la transmission se fait par aérosolisation (muqueuses, lésions cutanées) et nécessite un contact prolongé avec le patient infecté. Depuis l’arrêt de la vaccination contre la variole (Smallpox), il semblerait que la transmission soit facilitée, a priori dans le cadre d’une diminution de l’immunité secondaire. Notons que la transmission peut également se faire de mère à enfant, transplacentaire ou via contact direct post-accouchement. La transmission sexuelle n’est pour l’instant pas confirmée.
À ce jour, il existe deux “souches” Monkeypox – la souche d’Afrique centrale (Central African clade), du basin congolais, qui traditionnellement résulté un des symptômes plus sévères et est responsable des épidémies, et la souche du Cameroun (Cameroon clade).
Symptômes
Comme pour toute virose, un état fébrile accompagné d’un syndrome grippal (maux de tête, douleurs musculaires, maux de dos, gonflement des ganglions lymphatiques, frissons et épuisement) est décrit comme prodrome. S’en suit généralement une éruption cutanée (ou rash) qui se développe dans les 1-3 jour post-apparition de fièvre: l’éruption cutanée, initialement maculaire (de type érythème), évolue progressivement en vésicule et pustule, avant de former une croûte (qui tombe par la suite). Les symptômes cutanés commencent en général sur le visage (95% des cas), les extrémités (paume de la main et paume de pieds, ca. 75% des cas), es muqueuses (ca. 70% des cas) et conjonctives (ca. 20%) est également affecté , puis s’étendent à d’autres parties du corps, y compris les organes génitaux.
Spontanément résolutive après 2-4 semaines, la mortalité est souvent due à une surinfection cutanée voire ORL. La période d’incubation est généralement de 6 à 16 jours, mais peut aller jusqu’à 21 jours, avec une période infectieuse (contamination/transmissible) avant l’apparition des lésions cutanées, durant la phase de syndrome grippal. Lorsque la croûte tombe, la personne n’est plus infectieuse.
Notons que chez les patients homosexuels cas récemment décrit, les vésicules affectent particulièrement la zone génitale.
Complications
D’après l’OMS:
- Cas suspect: maladie aiguë avec une fièvre >38,3⁰C, des céphalées intenses, une lymphadénopathie, des douleurs dorsales, myalgie et asthénie intense, suivie d’un à trois jours plus tard d’une éruption cutanée se développant en commençant souvent sur le visage (le plus dense) et s’étendant ensuite ailleurs sur le corps, y compris la plante des pieds et la paume des mains.
- Cas probable: réponds à la définition de cas clinique, qui n’est pas confirmé en laboratoire, mais qui a un lien épidémiologique avec un cas confirmé ou non.
- Cas confirmé: un cas cliniquement compatible qui est confirmé en laboratoire.
Diagnostic
Les Orthopoxvirus étant sérologiquement cross réactionnel, la détection par antigène et anticorps ne permet pas de confirmer un diagnostic, en particulier chez les patients ayant sinon reçu un vaccin contre la variole. Le diagnostic se fait donc par analyse PCR d’une lésion cutanée/buccale (frottis ou biopsie) .
En Suisse, l’échantillon sera envoyé au Centre national de Référence des Infections Virales Emergentes (CRIVE), a Genève, dans une enveloppe triple-protégée (categorie B UN 3373 (triple emballage)).
Déclaration OFSP
Comme dans la plupart des pays, une déclaration auprès des instances de santé est obligatoire; en Suisse, en cas de suspicion (voir « cas suspect » ci-dessus), la déclaration doit être faite dans les 2 heures, par téléphone, et fiche officielle de déclaration.

Traitement
Le traitement est principalement symptomatique. Dans les cas sévères, un traitement antiviral, le Tecovirimat, peut être administré sur avis spécialisé. Ce traitement n’est actuellement pas autorisé en Suisse et n’est pas disponible.
Prévention
L’isolement est le moyen préventif de transmission le plus fiable, et doit être maintenu jusqu’au moment où les dernières vésicules se sont transformées en croûtes.
Pour toute personne appel a côtoyé un patient potentiellement infect, le port de masque, d’une surblouse et de gants est recommandé
Il n’y a pas de recommandation de mise en quarantaine des contacts étroits (définis comme suit: personnes vivant sous le même toit, soignants avec contact direct sans matériel de protection, contacts intimes alors que la personne est symptomatique et jusqu’au moment où les dernières vésicules se sont transformées en croûtes).
Notons que, comme précédemment décrit, la vaccination contre la variole humaine a été démontrée par plusieurs études d’observation comme étant efficace à environ 85 % pour prévenir la variole du singe, et un vaccin à virus vivant atténué qui a été approuvé par la Food and Drug Administration en 2019 pour la prévention de la variole du singe (Imvamune ou Imvanex) (non disponible en Suisse).
Bibliographie
OFSP. https://www.bag.admin.ch/bag/fr/home/krankheiten/krankheiten-im-ueberblick/affenpocken.html
Hopitaux Universitaire de Geneve. https://www.hug.ch/centre-maladies-virales-emergentes/variole-du-singe-monkeypox
OMS. https://www.who.int/news-room/fact-sheets/detail/monkeypox
ECDC. https://www.ecdc.europa.eu/en/news-events/monkeypox-cases-reported-uk-and-portugal
Di Giulio DB, Eckburg PB. Human monkeypox: an emerging zoonosis. Lancet Infect Dis. 2004 Jan;4(1):15-25. doi: 10.1016/s1473-3099(03)00856-9. Erratum in: Lancet Infect Dis. 2004 Apr;4(4):251.
McCollum AM, Damon IK. Human monkeypox. Clin Infect Dis. 2014 Jan;58(2):260-7. doi: 10.1093/cid/cit703. Epub 2013 Oct 24. Erratum in: Clin Infect Dis. 2014 Jun;58(12):1792.